醫(yī)學院沈曉驊課題組在非編碼RNA的染色質(zhì)結(jié)合機制研究中取得重要進展
清華新聞網(wǎng)3月12日電 3月12日,,清華大學醫(yī)學院沈曉驊教授團隊在《自然》(Nature)雜志上在線發(fā)表了題為 “U1 snRNP調(diào)控非編碼RNA的染色質(zhì)滯留”(U1 snRNP regulates chromatin retention of noncoding RNAs)的研究論文,,首次報道了U1 snRNP廣泛調(diào)控非編碼RNA在染色質(zhì)上的結(jié)合和移動的新機制,。
哺乳動物基因組的廣泛轉(zhuǎn)錄產(chǎn)生了大量的非編碼RNA,,相比于細胞質(zhì)定位的蛋白編碼mRNA,,這些非編碼RNA如長鏈非編碼RNA(lncRNA),、啟動子和增強子關(guān)聯(lián)的不穩(wěn)定轉(zhuǎn)錄本(uaRNA,、eRNA)等更傾向于結(jié)合染色質(zhì)參與調(diào)控染色質(zhì)結(jié)構(gòu)、轉(zhuǎn)錄和RNA加工等過程,。盡管零星報導少數(shù)RNA核滯留的現(xiàn)象,,但為何大部分lncRNA會滯留于染色質(zhì)上行使調(diào)控功能,仍是個不解之謎,。上世紀80年代初,,Joan Steitz通過系統(tǒng)性紅斑狼瘡患者血液抗體分離提取 U1,U2, U4, U5和U6小核糖核蛋白粒子(又稱為 snRNP),揭示了它們參與RNA剪接的經(jīng)典功能,。近年來施一公團隊系統(tǒng)報導了真核生物剪切體的原子結(jié)構(gòu)和生化功能,。然而,一直讓人困惑的是,,細胞內(nèi)U1 snRNP的數(shù)量為什么比其它剪接相關(guān)snRNP高 2-5倍,。雖然Gideon Dreyfuss和Phil Sharp等團隊曾揭示U1 snRNP調(diào)控轉(zhuǎn)錄終止和方向的非經(jīng)典功能,U1 snRNP在細胞中的豐富存在仍然是一個讓人困惑的問題,。
為了探究lncRNA的染色質(zhì)結(jié)合機制,,研究者首先建立和運用一套新穎的mutREL-seq方法來高精度篩選調(diào)控RNA定位的關(guān)鍵序列,意外發(fā)現(xiàn)了U1 snRNP識別位點參與調(diào)控候選RNA的染色質(zhì)滯留,。相比于蛋白編碼基因,,lncRNA轉(zhuǎn)錄本含有更多的U1識別位點(同時也是潛在的5’剪接供體位點),,而其基因組區(qū)域具有更少的3’剪接受體位點。并且U1 snRNP更高水平地結(jié)合在lncRNA上,。
隨后,,研究者分別使用antisense morpholino oligos(AMO)和auxin-induced degron(AID)誘導蛋白降解系統(tǒng),來抑制U1 snRNA和核心蛋白組分SNRNP70的功能,。研究者發(fā)現(xiàn)小鼠胚胎干細胞中近一半的lncRNA受U1 snRNP調(diào)控,。另外,與轉(zhuǎn)錄調(diào)控元件關(guān)聯(lián)的不穩(wěn)定非編碼轉(zhuǎn)錄本如uaRNA,、eRNA等,,它們的染色質(zhì)結(jié)合在U1 snRNP抑制后也顯著下降。研究者進一步證明了U1 snRNP直接調(diào)控成熟lncRNA與染色質(zhì)的結(jié)合,,而不是通過影響RNA合成,、加工或降解過程的動態(tài)變化所產(chǎn)生的間接影響。
機制上,,研究者鑒定了U1 snRNP在染色質(zhì)上的互作蛋白,,發(fā)現(xiàn)U1 snRNP結(jié)合特定磷酸化狀態(tài)的RNA轉(zhuǎn)錄聚合酶II(Pol II)。轉(zhuǎn)錄抑制明顯降低了U1 snRNP及其所調(diào)控的非編碼RNA與染色質(zhì)的結(jié)合,,表明U1 snRNP通過與磷酸化的Pol II互作來介導其互作RNA與染色質(zhì)的結(jié)合,。
最后,研究者通過以lncRNA Malat1為例,,進一步驗證了U1 snRNP對其染色質(zhì)結(jié)合的調(diào)控作用,。去除SNRNP70后,絕大部分Malat1 “核斑”定位信號消失,,并彌散在核質(zhì)及細胞質(zhì)中,。同時,Malat1在活躍表達基因染色質(zhì)區(qū)域的結(jié)合信號顯著下降,,表明U1 snRNP不僅可以將Malat1滯留在染色質(zhì)上,,同時也參與調(diào)控后者在染色質(zhì)上的移動及其與靶基因的結(jié)合。
綜上,,研究者提出如下模型(圖1):5’和3’剪接位點在lncRNA上的不對稱分布,,致使U1 snRNP持續(xù)結(jié)合在lncRNA轉(zhuǎn)錄本上,而不能通過RNA剪接過程釋放,,從而介導了lncRNA的染色質(zhì)滯留,。磷酸化Pol II進一步介導了lncRNA-U1 snRNP復合體在染色質(zhì)上的移動(mobilization)。對于大多數(shù)低豐度,、不穩(wěn)定的lncRNA,,它們只能靶向結(jié)合鄰近的染色質(zhì)區(qū)域(順式cis作用);而對于少數(shù)穩(wěn)定和高豐度的lncRNA,如Malat1,,U1 snRNP促進了其遷移和結(jié)合更多的靶基因區(qū)域(反式trans作用),。
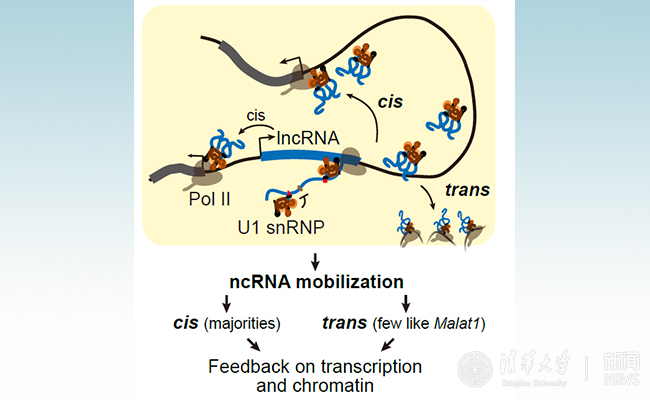
圖1. U1 snRNP介導非編碼RNA染色質(zhì)結(jié)合的模式圖。
該工作不僅揭示了U1 snRNP介導非編碼RNA在染色質(zhì)上功能和調(diào)控的新模式,,而且拓寬了U1 snRNP這一被廣泛研究的小核糖核蛋白粒子的新穎功能。
清華大學沈曉驊課題組的尹亞飛博士為本文的第一作者,。尹亞飛博士和沈曉驊教授為該論文的共同通訊作者,。沈曉驊課題組的博士生盧雨陽、張雪純,、邵雯和洪彥濤等參與了此項工作,。論文的其他研究者還包括清華大學生命學院張強鋒教授及其博士生李盼,中國科技大學的單革教授,,以及美國羅格斯大學新澤西醫(yī)學院(Rutgers New Jersey Medical School)的田斌教授,。該研究得到了國家自然科學基金委、科技部重點研發(fā)項目,、北京市高精尖中心及生命科學聯(lián)合中心等多個項目的支持,。
論文鏈接:
https://www.nature.com/articles/s41586-020-2105-3
供稿:醫(yī)學院
編輯:呂婷
審核:程曦
