清華柴繼杰研究組在《科學》發(fā)表論文
揭示NLRC4蛋白自抑制作用的分子機制
清華新聞網(wǎng)6月14日電 6月14日,清華大學生命科學學院柴繼杰教授研究組在國際頂級期刊《科學》(Science)在線發(fā)表題為《NLRC4蛋白自抑制機制的結構基礎》(Crystal structure of NLRC4 reveals its autoinhibition mechanism)的研究論文,首次報道了小鼠NOD樣受體NLRC4自抑制狀態(tài)的晶體結構,并通過結構分析和生化實驗揭示了該蛋白維持自抑制作用的分子機制,,這也是NOD樣受體家族中第一個被解析出的近乎全長的蛋白質晶體結構。
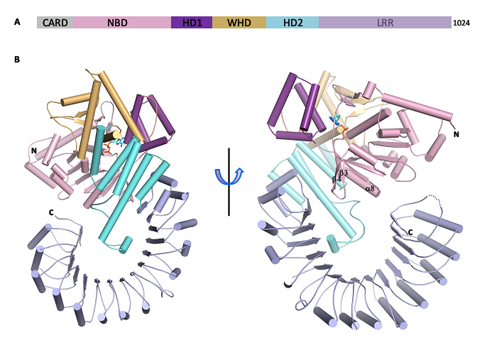
圖為小鼠NOD樣受體NLRC4自抑制狀態(tài)的晶體結構,。
清華大學生命科學學院柴繼杰教授為本文通訊作者,。鄭州大學常俊標教授,、哈爾濱工業(yè)大學黃志偉教授,、清華大學生命科學學院王佳偉副教授和鄧海騰教授也參與了此項工作。
NOD樣受體為近年來發(fā)現(xiàn)的一類位于細胞質內的模式識別受體,,能夠識別進入胞內的病原分子從而引起免疫應答,,是機體天然免疫系統(tǒng)的重要組成部分。NOD樣受體的異常與很多疾病密切相關,,包括如關節(jié)炎等各種自身免疫疾病,、肥胖等各種代謝綜合癥、炎癥性腸病以及腫瘤的發(fā)生,。對該家族蛋白作用機制的研究正成為基礎免疫學領域的一個重要的熱點領域,。
目前已經(jīng)鑒定出的NOD樣受體家族至少包含22種人類成員和34種鼠源成員。NLRC4是NOD樣受體家族中的一員,,主要識別細菌的鞭毛蛋白和III型分泌系統(tǒng)的成分,。NLRC4在正常情況下通過自抑制作用處于靜息狀態(tài);當病原體成分進入細胞內時,,被NLRC4識別從而使其活化,;活化的NLRC4發(fā)生自身多聚化,形成炎癥小體,,產(chǎn)生一系列的免疫應答反應。目前對NLRC4以及該家族其它蛋白是如何維持自抑制狀態(tài),、如何識別配體以及如何激活等問題都不清楚,。
柴繼杰教授領導的研究組一直以NOD樣受體家族的結構與功能作為主要研究方向,,經(jīng)過6年的不懈努力,終于獲得了小鼠NLRC4蛋白的晶體并通過X射線晶體衍射的方法解析了該蛋白分辨率為3.2 埃的晶體結構,。結構顯示單獨的NLRC4蛋白以單體的形式處于自抑制狀態(tài),。該蛋白中的核苷酸結合結構域(nucleotide-binding domain,NBD)結合的是ADP,,ADP介導的NBD同側翼螺旋結構域(winged-helix domain,,WHD)之間的相互作用對維持NLRC4的自抑制狀態(tài)十分關鍵。螺旋結構域2(helical domain 2,,HD2)通過和NBD中一段功能重要的α螺旋相互作用也參與了維持NLRC4的自抑制狀態(tài),。C末端的富含亮氨酸重復序列(leucine-rich repeat,LRR)結構域正好處于該蛋白發(fā)生多聚化的位置,,從而進一步保證自抑制狀態(tài)的維持,。當通過氨基酸突變的方法打破NBD-WHD、NBD-HD2或NBD-LRR之間的相互作用后,,這些突變體在細胞內組成型激活NLRC4,。以上的結構和生化結果表明,NLRC4蛋白是通過以NBD為中心多個結構域協(xié)同的方式維持自抑制狀態(tài),。NLRC4蛋白自抑制作用分子機制的揭示不僅加深了對該家族蛋白靜息狀態(tài)維持機制的認識,,也為了解一些疾病相關突變體異常激活的原因提供了重要線索。
上海同步輻射光源以及日本KEK光子工廠為數(shù)據(jù)收集提供了及時有效的支持,。
附 論文鏈接地址:
http://www.sciencemag.org/content/early/2013/06/12/science.1236381.full.pdf
供稿:生命學院 編輯:襄樺
